動物實驗的爭議與未來—Andrew Knight教授講座報導之一
2025.09.15
文:蔡育琳 圖:台灣動物平權促進會、好好愛牠協會、Andrew Knight

2025年8月最後兩天,台灣動物平權促進會與好好愛牠協會共同舉辦「當動物被使用,我們有哪些選擇?以國際視角,開啟動物倫理新對話」系列講座,主講者為英國獸醫與動物福利專家安德魯・奈特(Andrew Knight)教授,他從關心人權轉為關注動物,是一位優秀學者更是積極行動者。
8月30日上午的第一場講座,先由台灣愛鼠協會理事長張勝鬘介紹台灣動物實驗現況,再由奈特教授講述動物實驗的爭議與未來,包括科學評估、倫理原則、制度偏誤與替代方式等,引領大家一起思考動物實驗是否合理?
8月30日上午的第一場講座,先由台灣愛鼠協會理事長張勝鬘介紹台灣動物實驗現況,再由奈特教授講述動物實驗的爭議與未來,包括科學評估、倫理原則、制度偏誤與替代方式等,引領大家一起思考動物實驗是否合理?
台灣動物實驗需要更多監督管理

張勝鬘首先感謝大家關心鼠類,在動物實驗中90%以上都是犧牲鼠類動物。從2013至2023年,台灣的實驗動物使用量約110–170萬隻,死亡率大多超過70%,值得注意的是,為何多年來趨勢沒有變動、數字沒有變少?而在整體侵入性實驗中,只有77.69%使用麻醉或止痛,使用量最多的鼠類,止痛和麻醉只佔50%,痛苦程度偏高。
「我們在查核的時候,看到竟然有一隻小鼠一天要戳上40針,40次的抽取或注射,沒有麻醉,沒有任何疼痛的控制。」說到查核,張勝鬘也介紹IACUC(實驗動物照護與使用委員會),目前台灣各機構共有197個IACUC,分為內部和外部審核。
內部審核是機構的自我審核,外部審核則由60–70位委員組成(動保團體佔5位),因為人力有限,每年抽查約40家機構,平均4、5年才會輪到一次。外部查核會打分數但缺乏影響力,張勝鬘直言:「有人拿到較差十幾年了,但沒有改善過……講白了就是沒有作用。」

關於實驗動物的來源及繁殖,台灣目前是零管理,可能從繁殖場或寵物店購買動物,就帶回實驗室繁殖並實驗。張勝鬘表示:「這樣的動物實驗問題就是實驗根本不準,卻犧牲了每年百萬隻以上的動物。」(註:動物的遺傳基因、健康狀況、飼養方式等因素,都會影響實驗的準確度。)
張勝鬘也介紹了一些改進,例如化妝品從2019年禁用動物實驗,健康食品的13種動物實驗有5種改為人體實驗。替代科技跨部會平台引進102種替代實驗方法,執行上卻不容易,張勝鬘說明:「因為這些替代方式太新了,或是跟研究報告難以結合,或是他們沒有把握,所以很難撼動原本做動物實驗的習慣。」
動物實驗的爭議:一致性或不一致性?

安德魯・奈特(Andrew Knight)教授的講題為「Critically Evaluating the use of Animals within Research」(對於研究中使用動物的批判性評估)。他首先說明,關於動物侵入性使用的法令政策,國際間大多採用功利主義式的「傷害–利益分析」(Harm-benefit analysis),以人類可能獲得的利益及動物必定受到的傷害來做權衡。
科學界支持動物實驗的理由包括:動物實驗對人類疾病非常重要,醫學研究必須仰賴動物實驗,人體的複雜性需要同等複雜的實驗動物做為研究模型,如果禁止動物實驗,醫學進展將嚴重受阻。
有些人則保持相反主張,回顧人類與動物反應不一致的案例,某些藥物會造成動物嚴重副作用或死亡,對人類卻是無害的,例如盤尼西林(Penicillin)、嗎啡(Morphine)、阿司匹靈(Aspirin)等,如果以現今法規進行動物實驗,都不可能上市讓人類使用。

反過來的情況則是,某些藥物通過了動物實驗,或已經上市販售,卻引發人類嚴重副作用甚至死亡,例如TGN1412(造成人類受試者器官衰竭)、Vioxx(引發服用者心臟疾病)、Thalidomide(導致新生兒肢體畸形)等。另外就是藥物的不良反應(副作用),在美國是第4至第6大死因,在英國每年導致1萬多人死亡。
2004年,英國和美國有幾位科學家提出呼籲,對動物實驗進行系統性的檢視。他們表示,醫師和民眾常認為動物實驗一定就有效,但這些看法來自零散的個案經驗,或缺乏實證支持的主張。應該對現有及未來的動物實驗進行正式評估,包括全面搜尋相關研究、隨機公正選取樣本、研究與排除的標準透明化、評估所有高品質證據,並將結果發表於醫學期刊。
動物實驗有用嗎?
奈特教授在研讀博士時就開始評論動物實驗,也做了系統性的檢視。他查閱了27篇動物實驗研究,其中20篇是評估對人類臨床醫學的貢獻,只有2篇研究顯示動物實驗有效益,但其中1篇的結論仍具有爭議。另外7篇是評估對人類毒性反應的貢獻,結果未能清楚證明動物實驗對於預測人類毒性反應(例如致癌性、致畸性)有實用性。
奈特教授以相關文獻說明,在76篇發表於頂尖期刊、被引用超過500次的動物研究中,只有36.8%在人體實驗中被複製,18.4%在人體實驗時被推翻,44.7%未進入人體實驗。最後只有10.5%獲准給病人使用,但也無法保證一定有助益,經過核准的藥物仍有可能導致不良反應(副作用),先前已經提過,這在美國是第4至第6大死因。

以黑猩猩做動物實驗,真的對人類有幫助嗎?
另一個案例是對於黑猩猩的侵入性實驗,2005年有7位美國研究者呼籲增加黑猩猩研究的經費。他們強調這類研究在愛滋病、肝炎與癌症研究中的重要性,也因為黑猩猩和人類的遺傳相似性,可做為理想的生醫研究範本。
奈特教授為了確認此事而檢視相關論文,從1995到2004年之間,找到749個與黑猩猩相關的研究,乍看似乎有許多貢獻。他隨機挑選了95篇黑猩猩研究,卻發現有47篇未曾被引用,34篇被其他動物研究引用,只有14篇被27篇人類醫學研究引用。但再檢視這27篇引用黑猩猩研究的醫學論文,有17篇是廣泛性的綜述論文(這類論文通常會引用大量文獻),黑猩猩研究只有極小的貢獻。而在對抗人類疾病的論文中,沒有一篇黑猩猩研究提供了顯著貢獻,甚至在多數情況下,都未能提供任何實質貢獻。
奈特教授向大家發問:「為什麼會這樣?科學界不是一直告訴我們,動物實驗對人類的健康很有貢獻嗎?」

奈特教授以有趣的圖片,表達對於動物實驗的疑惑。
奈特教授以相關文獻說明,在76篇發表於頂尖期刊、被引用超過500次的動物研究中,只有36.8%在人體實驗中被複製,18.4%在人體實驗時被推翻,44.7%未進入人體實驗。最後只有10.5%獲准給病人使用,但也無法保證一定有助益,經過核准的藥物仍有可能導致不良反應(副作用),先前已經提過,這在美國是第4至第6大死因。

另一個案例是對於黑猩猩的侵入性實驗,2005年有7位美國研究者呼籲增加黑猩猩研究的經費。他們強調這類研究在愛滋病、肝炎與癌症研究中的重要性,也因為黑猩猩和人類的遺傳相似性,可做為理想的生醫研究範本。
奈特教授為了確認此事而檢視相關論文,從1995到2004年之間,找到749個與黑猩猩相關的研究,乍看似乎有許多貢獻。他隨機挑選了95篇黑猩猩研究,卻發現有47篇未曾被引用,34篇被其他動物研究引用,只有14篇被27篇人類醫學研究引用。但再檢視這27篇引用黑猩猩研究的醫學論文,有17篇是廣泛性的綜述論文(這類論文通常會引用大量文獻),黑猩猩研究只有極小的貢獻。而在對抗人類疾病的論文中,沒有一篇黑猩猩研究提供了顯著貢獻,甚至在多數情況下,都未能提供任何實質貢獻。
奈特教授向大家發問:「為什麼會這樣?科學界不是一直告訴我們,動物實驗對人類的健康很有貢獻嗎?」

為何動物實驗無法準確?
奈特教授認為至少有5個原因:跨物種的差異、壓力性的環境與操作流程、慢性高劑量動物研究的偽陽性、方法學品質低落、發表偏誤與檔案櫃問題,這些因素都降低了動物實驗對人類臨床的預測力。
1. 跨物種的差異
人類和動物是不同物種,對疾病的易感性和進展不同,對藥物和毒素的吸收、代謝、療效也不同。此外,動物實驗可能使用近親繁殖、單一性別、年輕動物等設計,或是樣本數不足、缺乏動物多樣性。動物實驗缺乏人類的合併疾病或其他風險因素,而動物長期處在高壓環境中,身體機能和免疫系統也會失真,導致實驗無法準確。
2. 壓力性的環境與操作流程
從一開始取得動物、運送動物就會造成影響,再到實驗操作的嚴重程度和持續時間,以及麻醉與止痛藥的使用不足,讓動物承受了多重壓力。
奈特教授表示:「研究中心會說他們傷害動物的比例很低,但我們做過實驗的人都知道這不是真的。」實驗操作流程大多是侵入性的,包括會致死的操作(無論動物是否清醒)、外科手術、基因改造動物的過程。根據加拿大最近10年的數據,高度侵入性的操作約有29%至44%;而在英國1998年至2009年間,沒有麻醉的實驗操作約有59%至69%。
有學者在檢視了110項生醫文獻後做出結論,實驗動物長期在受限制和壓力性的環境中,會造成神經結構受損、行為異常、生理失調。相較於健康的動物,他們的學習、記憶、認知能力都會下降,也可能會憂鬱、增加攻擊性。使用不健康的動物做實驗,自然會影響實驗結果,環境「豐富化」或許能延遲問題,卻無法完全改善問題。
有學者評估了80篇研究,發現就算是常規的實驗操作,例如搬運、抓握、抽血、灌胃等,動物也會出現壓力、恐懼、痛苦等反應,這些是動物每天都要承受的,不會隨著時間而適應。奈特教授特別說明,胃管灌食(gavage)是用一個金屬的管子插入動物的食道再到胃部,這種操作很常見,他檢視了168個實驗,發現最常見的給藥方式是混入食物中(49.4%),第二常見的方式就是胃管灌食(33.3%)。
長期壓力會造成動物的免疫力下降,也可能出現刻板行為,例如過度理毛、攻擊行為、重複跳躍、咬籠條等,這些重複而無明顯目的的行為,被認為是動物深層的心理痛苦表現。由於囓齒類動物多為夜行性,研究者很難發覺這些行為的普遍程度。

實驗動物大多被關在狹小、簡陋的籠子,通常處於社交隔絕狀態,這種做法是為了標準化、減少環境變數、出於經濟考量。右圖這隻老鼠是少數幸運的實驗鼠,還有玩具可以玩。
3. 慢性高劑量囓齒類動物研究的偽陽性結果
偽陽性(false positives)的意思是指,某些物質在動物實驗中被認定有毒或致癌,但實際上對人類可能無害。囓齒類動物與人類有明顯的生理差異,包括代謝、DNA 修復、免疫反應等,人類可能對某些物質沒有反應,也因為人體的承受劑量比較高,但在動物身上可能會有反應並受害。
相反的,如果囓齒類動物對某些物質沒有反應,實驗者可能會想增加劑量。但在注射高劑量的物質後,可能導致動物的生理防禦機制失效,包括上皮細胞脫落、酵素系統和DNA修復失效等,當動物整體無法正常運作,就不會有真實的毒性反應。

講座現場有一位狗狗聽眾。
4. 方法學品質低落
奈特教授發現至少有11項系統性回顧指出,多數動物實驗的方法學品質不佳,常見缺失包括:未計算樣本數、樣本數不足、未隨機分組、未做盲法評估、未揭露利益衝突,導致研究結果偏差、效益高估。
有些動物實驗的結果相當客觀而明顯,可能不需要盲法評估,因為標準化的測量方式,操作者的主觀影響有限。但有些動物實驗的結果有高度主觀性,盲性評估就變得很重要,假如操作者知道動物屬於哪一個處理組別,可能會放大或忽略某些反應,導致觀察的偏差。
當實驗者有預期特定的結果、測量主觀的變因,或是有誘因去產出符合預測的數據,偏差的風險最為強烈。在一篇急診醫學的動物研究回顧中發現,如果研究採用隨機分配和盲性評估,治療效果會顯著降低;如果研究沒有採用這些方法,就往往會高估治療效果。
2010年,英國 NC3Rs(國家動物研究3Rs中心)推出 ARRIVE 指南(Animal Research: Reporting of In Vivo Experiments動物研究:活體實驗報告準則),以確保動物實驗的品質並符合3Rs原則。ARRIVE指南獲得了1000多家期刊支持,也有許多贊助單位,在國際間應該是最有公信力的。但根據瑞士的一項調查,在302位完成問卷的動物實驗研究者中,有56.3%從未聽過ARRIVE指南。
2020年,ARRIVE指南從20項減為10項。
5. 發表偏誤(publication bias)與檔案櫃問題(file drawer problem)
奈特教授先舉例說明,假設有研究者用藥物對老鼠做了20次實驗,19次沒有反應,1次有反應,研究者對有反應的結果會更興奮,這個結果也更有機會被發表。19次正確的反應沒有被刊出,反而是1次錯誤的反應被刊出,更糟糕的是,未來的學者在閱讀報告時,只會看到那1次反應,不知道有19次反應被束之高閣。
在一篇急性缺血性中風的動物研究中,分析16項系統性回顧、525篇出版物、1359項實驗,共使用19956隻動物,結果只有10篇(2%)沒有顯著療效。奈特教授說:「如果你要測試一種新藥物,發現有98%的成功機率,你不需要是個科學家也能看出不對勁。」
透過漏斗圖(Funnel plot)、Egger回歸分析(Egger regression)、修剪與填補法(Trim-and-fill plot)等調整,發現有214項(16%)實驗未被發表,可能因為結果不顯著、不符合預期,卻造成約3600隻動物死亡。平均而言,發表偏誤可能導致療效被高估1/3。奈特教授強調,發表偏誤的問題在所有科學領域都會發生,而動物實驗是唯一的領域,許多患者的病情會受到影響,還有許多動物會因此死亡。

結果不顯著、不符合預期的研究,通常不會被發表,而是被收進檔案櫃,造成文獻中只呈現正面結果,失去科學真實性。
1. 跨物種的差異
人類和動物是不同物種,對疾病的易感性和進展不同,對藥物和毒素的吸收、代謝、療效也不同。此外,動物實驗可能使用近親繁殖、單一性別、年輕動物等設計,或是樣本數不足、缺乏動物多樣性。動物實驗缺乏人類的合併疾病或其他風險因素,而動物長期處在高壓環境中,身體機能和免疫系統也會失真,導致實驗無法準確。
2. 壓力性的環境與操作流程
從一開始取得動物、運送動物就會造成影響,再到實驗操作的嚴重程度和持續時間,以及麻醉與止痛藥的使用不足,讓動物承受了多重壓力。
奈特教授表示:「研究中心會說他們傷害動物的比例很低,但我們做過實驗的人都知道這不是真的。」實驗操作流程大多是侵入性的,包括會致死的操作(無論動物是否清醒)、外科手術、基因改造動物的過程。根據加拿大最近10年的數據,高度侵入性的操作約有29%至44%;而在英國1998年至2009年間,沒有麻醉的實驗操作約有59%至69%。
有學者在檢視了110項生醫文獻後做出結論,實驗動物長期在受限制和壓力性的環境中,會造成神經結構受損、行為異常、生理失調。相較於健康的動物,他們的學習、記憶、認知能力都會下降,也可能會憂鬱、增加攻擊性。使用不健康的動物做實驗,自然會影響實驗結果,環境「豐富化」或許能延遲問題,卻無法完全改善問題。
有學者評估了80篇研究,發現就算是常規的實驗操作,例如搬運、抓握、抽血、灌胃等,動物也會出現壓力、恐懼、痛苦等反應,這些是動物每天都要承受的,不會隨著時間而適應。奈特教授特別說明,胃管灌食(gavage)是用一個金屬的管子插入動物的食道再到胃部,這種操作很常見,他檢視了168個實驗,發現最常見的給藥方式是混入食物中(49.4%),第二常見的方式就是胃管灌食(33.3%)。
長期壓力會造成動物的免疫力下降,也可能出現刻板行為,例如過度理毛、攻擊行為、重複跳躍、咬籠條等,這些重複而無明顯目的的行為,被認為是動物深層的心理痛苦表現。由於囓齒類動物多為夜行性,研究者很難發覺這些行為的普遍程度。

3. 慢性高劑量囓齒類動物研究的偽陽性結果
偽陽性(false positives)的意思是指,某些物質在動物實驗中被認定有毒或致癌,但實際上對人類可能無害。囓齒類動物與人類有明顯的生理差異,包括代謝、DNA 修復、免疫反應等,人類可能對某些物質沒有反應,也因為人體的承受劑量比較高,但在動物身上可能會有反應並受害。
相反的,如果囓齒類動物對某些物質沒有反應,實驗者可能會想增加劑量。但在注射高劑量的物質後,可能導致動物的生理防禦機制失效,包括上皮細胞脫落、酵素系統和DNA修復失效等,當動物整體無法正常運作,就不會有真實的毒性反應。

4. 方法學品質低落
奈特教授發現至少有11項系統性回顧指出,多數動物實驗的方法學品質不佳,常見缺失包括:未計算樣本數、樣本數不足、未隨機分組、未做盲法評估、未揭露利益衝突,導致研究結果偏差、效益高估。
有些動物實驗的結果相當客觀而明顯,可能不需要盲法評估,因為標準化的測量方式,操作者的主觀影響有限。但有些動物實驗的結果有高度主觀性,盲性評估就變得很重要,假如操作者知道動物屬於哪一個處理組別,可能會放大或忽略某些反應,導致觀察的偏差。
當實驗者有預期特定的結果、測量主觀的變因,或是有誘因去產出符合預測的數據,偏差的風險最為強烈。在一篇急診醫學的動物研究回顧中發現,如果研究採用隨機分配和盲性評估,治療效果會顯著降低;如果研究沒有採用這些方法,就往往會高估治療效果。
2010年,英國 NC3Rs(國家動物研究3Rs中心)推出 ARRIVE 指南(Animal Research: Reporting of In Vivo Experiments動物研究:活體實驗報告準則),以確保動物實驗的品質並符合3Rs原則。ARRIVE指南獲得了1000多家期刊支持,也有許多贊助單位,在國際間應該是最有公信力的。但根據瑞士的一項調查,在302位完成問卷的動物實驗研究者中,有56.3%從未聽過ARRIVE指南。

5. 發表偏誤(publication bias)與檔案櫃問題(file drawer problem)
奈特教授先舉例說明,假設有研究者用藥物對老鼠做了20次實驗,19次沒有反應,1次有反應,研究者對有反應的結果會更興奮,這個結果也更有機會被發表。19次正確的反應沒有被刊出,反而是1次錯誤的反應被刊出,更糟糕的是,未來的學者在閱讀報告時,只會看到那1次反應,不知道有19次反應被束之高閣。
在一篇急性缺血性中風的動物研究中,分析16項系統性回顧、525篇出版物、1359項實驗,共使用19956隻動物,結果只有10篇(2%)沒有顯著療效。奈特教授說:「如果你要測試一種新藥物,發現有98%的成功機率,你不需要是個科學家也能看出不對勁。」
透過漏斗圖(Funnel plot)、Egger回歸分析(Egger regression)、修剪與填補法(Trim-and-fill plot)等調整,發現有214項(16%)實驗未被發表,可能因為結果不顯著、不符合預期,卻造成約3600隻動物死亡。平均而言,發表偏誤可能導致療效被高估1/3。奈特教授強調,發表偏誤的問題在所有科學領域都會發生,而動物實驗是唯一的領域,許多患者的病情會受到影響,還有許多動物會因此死亡。

結論:倫理與科學的再平衡

奈特教授總結道,因為歷史、當代典範或某些習慣,動物實驗被認為可預測人類實驗的結果,在毒性測試和生醫研究中提供了基礎。但動物實驗持續被使用,主要是歷史與文化原因,而非科學驗證有效,例如許多監管單位覺得「使用動物數據比較安心」,還有些人認為「在動物身上做測試,自然就會有效」。
然而多數系統性的評估已經顯示,動物實驗無法充分預測人類實驗,在臨床介入開發、人類毒性評估中,都難以提供實質利益。此外,動物實驗消耗了大量財物、人力和科學資源,對於促進人類健康是一種極度低效的方式,更佔用了其他以人為本的研究資源。
當考量整體的代價與利益時,我們無法合理斷言,人類的利益能超過動物承受的代價,無論是對於病患、消費者、出於科學好奇或利益驅動的人。現有的證據顯示,人類實際的利益幾乎從未讓這些代價正當化。只有在極度不平等的情況下,才能說動物實驗在倫理上是合理的,也就是將人類微小或偶發的利益,看得比動物普遍承受的痛苦更為重要。
儘管動物實驗的價值被質疑,仍然得到大量批准,奈特教授認為,倫理審查委員會(Ethics committees)在倫理監督上是失職的,他們基於錯誤的獲利假設,未能盡到服務社會的責任,也辜負了他們應該保護的動物。
動物實驗的未來:3Rs原則、替代方案

1959 年,William Russell和Rex Burch兩位學者提出動物研究3Rs原則。
1. 替代(Replacement):盡可能以非動物方法取代動物使用,這是最重要的。
2. 減量(Reduction):將動物數量減至最低。
3. 精緻化(Refinement):避免或減少動物的痛苦和壓力,並提升福祉。
奈特教授說明,提升福祉是一個近期才有的觀念,以前對動物福利的想像只是避免負面影響,現在我們知道也要讓動物有機會接受正向影響。其它延伸的原則包括:再利用(Re-use)、回收(Recycling)、恢復或安置(Rehabilitation)。
說到動物實驗的替代方案,奈特教授認為,在進行新研究之前,應加強數據的共享與評估機制,許多藥廠將研究結果當成商業機密,對於公共利益毫無幫助。我們應該促成一些措施和動機,讓藥廠在幾年後公布數據或得到補償。
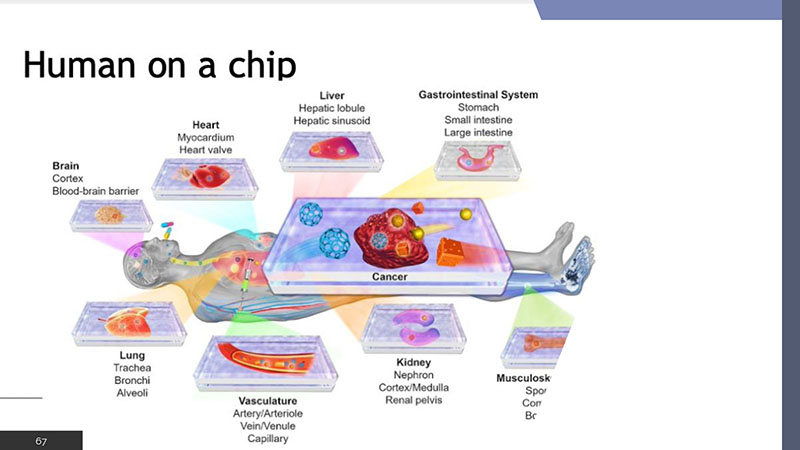
其他替代方案包括:物理化學評估與電腦模擬(如QSARs、專家系統)、化學分組與交叉推論(read-across)、生理基礎藥物動力學模型(PBPK)、人類肝細胞培養與代謝活化系統、體外分析方法、組織培養技術、晶片系統(細胞、器官、人體)、微陣列技術(microarray technology)、微劑量(microdosing)臨床實驗、高階影像技術、人類流行病學、社會學與心理學研究等。
奈特教授表示,目前的科學無法回答關於人類的所有問題,人體實驗有限制,但動物實驗有更多限制,替代方案也有限制,但動物實驗的發展潛力更低。使用人體或人類組織的替代方案,可以產生更快速、更便宜的結果,更能準確預測人類反應,未來發展也更讓人期待。

Andrew Knight教授推薦閱讀書籍
1.《The Costs and Benefits of Animal Experiments》(2011)Andrew Knight教授著作
2.《Animal Experimentation: Working Towards a Paradigm Change》(2019)Andrew Knight教授為作者群之一
3.《Routledge Handbook of Animal Welfare》(2023)Andrew Knight教授為主編之一
2.《Animal Experimentation: Working Towards a Paradigm Change》(2019)Andrew Knight教授為作者群之一
3.《Routledge Handbook of Animal Welfare》(2023)Andrew Knight教授為主編之一
相關連結
-Andrew Knight(Andrew Knight教授個人網站)
-Animal Experiments Info(Andrew Knight教授建立的網站,提供動物實驗的效益、爭議、替代等資訊)
相關報導
-Animal Experiments Info(Andrew Knight教授建立的網站,提供動物實驗的效益、爭議、替代等資訊)
相關報導
推薦文章
